理想気体 関連問題 【広告】ここから広告です。ご覧の皆さまのご支援ご理解を賜りたく、よろしくお願いいたします。
【広告】広告はここまでです。
気体が、以下の特徴を有するときに、 理想気体 と言う。 (1) 気体を構成する分子の大きさが無視できる。
(2) 気体を構成する分子間に働く力が無視できる。
理想気体では、 ボイル・シャルルの法則 が成立し、その 圧力 を p , 体積 を V ,モル数を n , 気体定数 を R , 絶対温度 を T として、 状態方程式 : 圧力 p は、気体と接触している面の 面積 を S ,この面にかかる 力 を F として、 で与えられます。 力 の単位を [N] , 面積 の単位を [ として、 圧力 の単位は [ となりますが、これを [Pa] (‘ パスカル ' と読む ) という単位で表します。 です。つまり、 1[ の面に 1[N] の 力 が働くときに、気体の 圧力 は 1[Pa] となります。 [hPa] (‘ ヘクトパスカル ' と読む ) という単位を 気圧 の単位として用いますが、 です。 1 気圧 (1[atm] と書く。 atm は、 ‘ アトム ' と読む ) 、という単位も用いられます。 という関係があります。 温度 を考えるときには、 絶対温度 で考えます。 摂氏温度 t [と 絶対温度 T [K] (‘ケルビン ' と読みます ) との間には、 という関係があります。 0[ , 1[atm] の気体の状態を「標準状態」と言います。 気体分子の量 を [mol] という単位で考えます。 0.012[Kg] の炭素 12 ( と書きます。原子量 12 の炭素原子 ) の原子の個数を 1[mol] と定義します。 1[mol] の気体の原子の個数は、ほぼ ( アボガドロ数 と言う ) です。また、標準状態の理想気体 1[mol] の占める 体積 が、 22.414[ であることが知られています。 温度 を上げるか 圧力 を下げるかすると、 圧力 p と 体積 V と 絶対温度 T の間に、 という関係が成り立つようになります。これを、 ボイル・シャルルの法則 と呼びます。 1[mol] の気体の場合、一定値は気体の種類によらずある定数 R になります。この定数 R を 気体定数 と呼び、ほぼ、 n [mol]あるとして、 状態方程式 : (1[mol] 当たりの 体積 ) として、近似的に、 van der Waals の状態方程式: ( 但し、 a , b は定数 ) が成り立つことが知られています。 1 原子で気体分子ができている気体、水素のような 2 原子で気体分子ができている気体では、 a , b の値は無視できるほど小さく、ほぼ理想気体としての振る舞いをします。ヘリウム、ネオン、水素では、上記の理想気体の条件 (1) , (2) が成り立っています。 1 原子で気体分子ができている気体を特に、 単原子分子理想気体 と言います。 状態方程式 : において、 絶対温度 T が一定であるとき、 が成り立ちます。これを ボイルの法則 と言います。理想気体では、温度一定 の条件下で、 圧力 と 体積 が反比例します。 状態方程式 : において、 圧力 p が一定 であるとき、 体積 と 絶対温度 は比例します。これを シャルルの法則 と言います。この事実は、気体の 温度 を下げていくと、どんどん 体積 が減り続け、仮に気体のままでいるのであれば ( 実際には、相変化を起こして、液体、もしくは、固体になってしまいます ) 、いずれ 体積 は 0 になってしまうことを意味しています。この 体積 0 になってしまう 温度 ( 摂氏 ) を、 絶対温 度 0[K] としています。 【広告】ここから広告です。ご覧の皆さまのご支援ご理解を賜りたく、よろしくお願いいたします。
【広告】広告はここまでです。
物理基礎事項 TOP 物理 TOP TOP ページに戻る 【広告】ここから広告です。ご覧の皆さまのご支援ご理解を賜りたく、よろしくお願いいたします。
【広告】広告はここまでです。 各問題の著作権は © 2005-2024 (有)りるらる 苦学楽学塾 随時入会受付中! 理系大学受験ネット塾 苦学楽学塾 (ご案内はこちら )ご入会は、こちらまでメール を 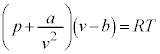 (但し、a,bは定数)
(但し、a,bは定数)